COVID-19 : Des nano-leurres pour occuper le virus
Ces bioingénieurs de la North Carolina State University développent des leurres nanométriques ou nanoleurres de la protéine ACE2 présente sur les cellules hôtes, et sur laquelle se « plugge » le coronavirus SARS-CoV-2 pour les infecter. Dérivés de cellules sphéroïdes pulmonaires humaines (LSC) ces nanoleurres peuvent se lier et neutraliser le SRAS-CoV-2. En « faisant diversion, ils protègent les cellules pulmonaires de l'hôte contre l'infection. Ces travaux publiés dans la revue Nature Nanotechnology montrent, chez le macaque ces « fantômes » cellulaires augmentent de manière exponentielle la surface des faux sites de liaison pour piéger le virus.
Fabriqués à partir de cellules sphéroïdes pulmonaires humaines, les nanoleurres se montrent ici efficace sur le macaque modèle de COVID-19 à se lier au SARS-CoV-2 et à le neutraliser, en favorisant la clairance virale et en limitant considérablement les lésions pulmonaires. En imitant le récepteur auquel le virus se lie plutôt que de cibler le virus lui-même, la thérapie par nanoleurres promet également d’être efficace contre les variantes émergentes du virus.
Le SRAS-CoV-2 se lie aux nanoleurres, plus nombreux plutôt qu’à la cellule hôte
Le SRAS-CoV-2 pénètre dans une cellule lorsque sa protéine de pointe se lie au récepteur de l'enzyme de conversion de l'angiotensine 2 (ACE2) à la surface de la cellule. Les LSC, une combinaison naturelle de cellules souches épithéliales pulmonaires et de cellules mésenchymateuses expriment également la protéine ACE2. C’est à partir de ces LSC que les scientifiques développent ces nanoleurres, en les convertissant en nanovésicules, de minuscules bulles entourées d’une membrane cellulaire avec des récepteurs ACE2 et d'autres protéines spécifiques aux cellules pulmonaires à leur surface.
« De fausses serrures qui se lient et piègent le virus, l'empêchant d'infecter les cellules hôtes et de se répliquer, et le système immunitaire du corps s'occupe du reste »,
résume l’auteur principal, le dr Ke Cheng, professeur émérite de médecine régénérative à la North Carolina State University et professeur de génie biomédical à Chapel Hill.
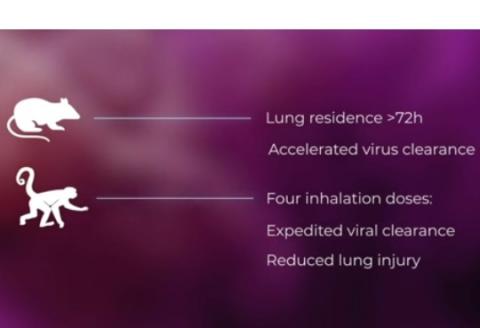
La protéine de pointe du virus se laisse abuser et se lie aux récepteurs ACE2 sur les leurres, montre l’équipe de recherche, in vitro, puis chez une souris modèle à qui les leurres ont été délivrés par inhalation. Chez la souris, ces nanoleurres restent environ 72 heures dans les poumons, suffisamment longtemps pour accélérer la clairance virale. Enfin, 3è étape, chez un modèle macaque, la thérapie par inhalation accélère également la clairance virale et réduit l'inflammation et la fibrose dans les poumons.
- Aucune toxicité n’est constatée chez la souris ou le macaque, mais cela reste à confirmer par de futurs essais cliniques de phase I chez l’Homme.
1 LCS peut générer environ 11.000 nanoleurres, c’est le deuxième atout spectaculaire de cette stratégie thérapeutique. Et le déploiement de millions de ces leurres augmente de manière exponentielle la surface des faux sites de liaison pour piéger le virus,
leur petite taille les transforme essentiellement en petites « collations » pour les macrophages qui n’en font qu’une bouchée.
Mais ce n’est pas tout : 3 autres avantages thérapeutiques sont mis en avant par ces scientifiques :
- les nanoleurres peuvent être délivrés de manière non invasive aux poumons par inhalation ;
- étant acellulaires, les nanoleurres peuvent être facilement conservés avec une grande stabilité et sur une longue durée ;
- les LSC sont déjà utilisées dans d'autres essais cliniques, leur utilisation dans ce contexte pourrait donc être facilité
Le paradigme ici est de se concentrer sur les défenses du corps plutôt que sur le virus qui va d’ailleurs continuer à muter, soulignent les auteurs.